Grupo de Neuroingeniería Biomédica
| Responsable | Eduardo Fernández Jover |
RESUMEN DE LA INVESTIGACIÓN
Somos un grupo multidisciplinar compuesto por especialistas en diversos campos como la ingeniería, biología, la informática, la robótica, la medicina, etc. Nuestro principal objetivo es la investigación básica y aplicada en patologías visuales, optogenética, estudio de terapias frente a neuropatías de tipo visual, el diseño y desarrollo de dispositivos y sistemas robóticos que ayuden a mejorar la capacidad cognitiva y comunicativa, la salud y la capacidad física de las personas que padecen discapacidades motrices y sensoriales.
LÍNEAS DE INVESTIGACIÓN
Línea 1: Desarrollo y validación de un modelo de neovascularización coroidal inducido por láser
El modelo de neovascularización coroidea inducida por láser es un método establecido utilizado para evaluar las terapias para la degeneración macular húmeda relacionada con la edad (AMD húmeda), una de las principales causas de ceguera en nuestra población de adultos mayores. El principal objetivo de esta línea es obtener un modelo validado para experimentar terapias y tratamientos para el control y curación de esta patología con la finalidad de pasar en el futuro a fases clínicas en humanos con los tratamientos ensayados en el modelo animal.
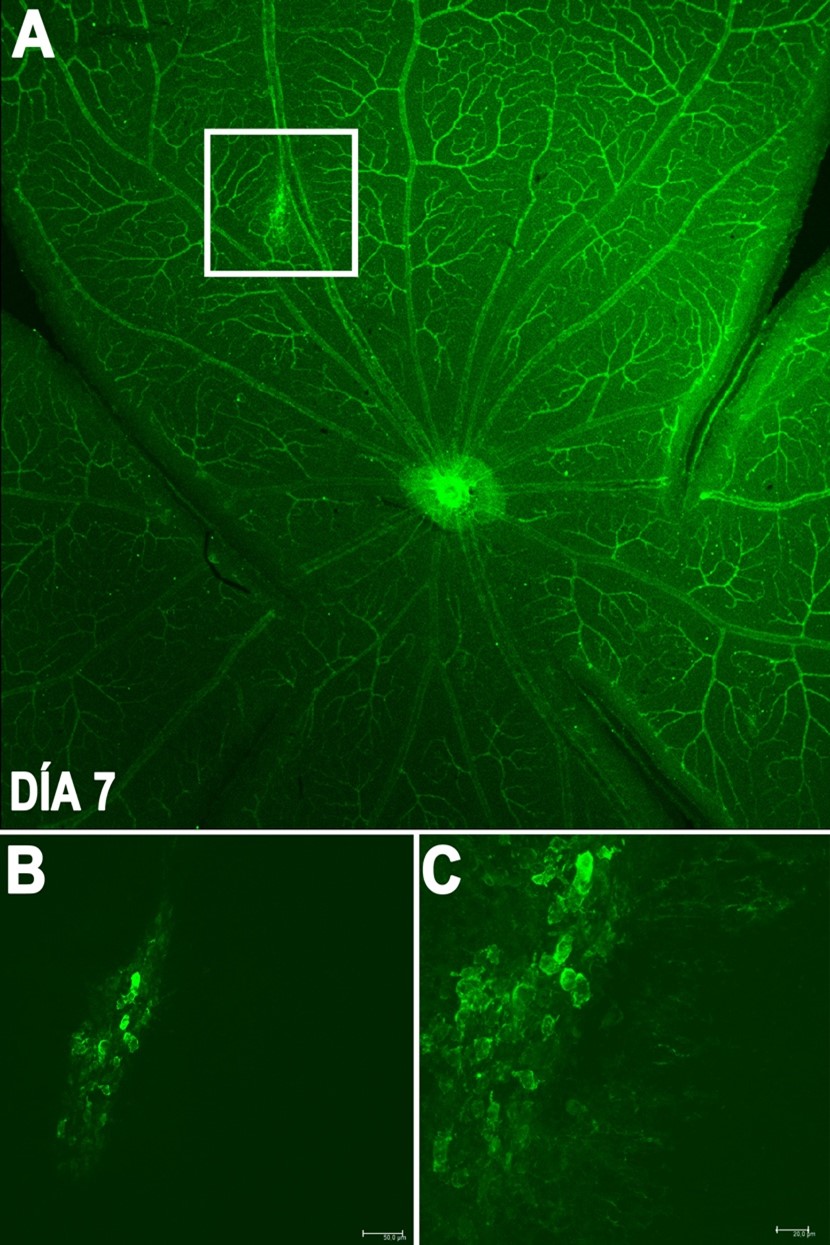
Generación de neovascularización mediante un sistema láser en retina de rata tras 7 días.
Línea 2:Terapia oftalmológica mediante RNA de interferencia (siRNA) y anticuerpos monoclonales humanizados para patologías degenerativas retinianas.
Esta línea de investigación se basa en la aplicación de nuevas moléculas basadas en RNA de interferencia y anticuerpos monoclonales humanizados para patologías crónicas como la degeneración macular asociada a la edad (DMAE), la retinopatía diabética y la retinitis pigmentaria, que actualmente carecen de tratamientos satisfactorios.
Línea 3: DRUG4SIGHT: Light-regulated drugs to restore sight
En las enfermedades degenerativas de la retina como la retinitis pigmentosa, las células fotorreceptoras se pierden progresivamente, lo que conduce a una discapacidad visual con opciones de tratamiento limitadas. Esta línea pretende caracterizar una serie de compuestos activos sensibles a la luz que puedan fotosensibilizar la retina, estimulando proteínas aún presentes en la retina degenerada y hacer actuar los receptores remanentes de células no degeneradas.
Línea 4: Nueva generación de lentes intraoculares multifuncionales que permiten la liberación prolongada y controlada de agentes terapéuticos a nivel intraocular (OCULUS)
Para evitar o disminuir efectos asociados a la cirugía de cataratas (dolor, infección, inflamación y posibles hemorragias intraoculares) es necesario administrar diariamente fármacos antiinflamatorios y antiinfecciosos durante al menos 6-8 semanas tras la cirugía. La administración tópica de estos fármacos logra retener menos del 5 % del fármaco aplicado tras atravesar la córnea. Por ello, esta línea de investigación se centra en el desarrollo de nuevas lentes intraoculares que liberan sostenidamente fármacos con el fin de obtener una dosis terapéutica continuada.
Línea 5: Aplicación de biofilms con Timolol para el control de la presión intraocular (OCULIPID)
El glaucoma es una enfermedad visual progresiva cuyo factor de riesgo más importante es la elevación de la presión intraocular. Las formulaciones farmacéuticas oculares actuales presentan inconvenientes en cuanto a su administración y eficacia terapéutica. Esta línea de investigación se centra en la aplicación tópica de biofilms lipídicos formulados con Timolol de liberación prolongada para el control de la presión intraocular en un modelo experimental preclínico de glaucoma de conejo.
Línea 6: Entorno de modelado computacional para la evaluación de la seguridad y eficacia de la estimulación del sistema nervioso periférico
El objetivo de esta línea es desarrollar y poner a disposición de la comunidad científica un marco de modelado computacional modular, integrado y multiescala que permitirá diseñar neuroestimuladores periféricos seguros y eficaces. La consecución de esta línea se realizará mediante la reconstrucción tridimensional de la microestructura de nervios estimulados, a través de secciones histológicas, por un método de disección anatómica asistida por computadora. Con ello se pretende mejorar la descripción de la distribución de las fibras nerviosas, proporcionar una representación 3D precisa de los nervios ciáticos, y desarrollar una base de datos informatizada de la topografía de las fibras nerviosas.
Línea 7: Terapia génica con vectores no virales para el tratamiento de enfermedades neurodegenerativas
A día de hoy, la cura de las enfermedades neurodegenerativas es un problema médico que está lejos de resolverse. Un enfoque para lograr una solución es la capacidad de reemplazar los genes defectuosos involucrados en el desarrollo de tales enfermedades por nuevos genes completamente funcionales capaces de interrumpir su progresión. La terapia génica consiste en la transferencia de material genético exógeno para la modificación de células con fines terapéuticos o de investigación. En colaboración con el grupo NanoBioCel (Grupo de Micro y Nano Tecnologías, Biomateriales y Células) de la Universidad del País Vasco, nuestro grupo está trabajando en el desarrollo de nuevos vectores no virales para transferir material genético al interior de las células del sistema nervioso en Con el fin de encontrar nuevas terapias para enfermedades neurológicas. Las grandes ventajas de los vectores no virales en comparación con otros enfoques son su muy baja o nula respuesta inmunogénica en los organismos receptores, su seguridad biológica y química para científicos y fabricantes, su capacidad para transportar grandes fragmentos genéticos dentro de las células y también , su facilidad de producción, manejo, almacenamiento y bajo costo de producción.
Línea 8: Desarrollo de Neuroprótesis Visuales
El equipo multidisciplinar del NBIO, dirigido por el Prof. Eduardo Fernandez Jover, está formado por un grupo de médicos, cirujanos, biólogos e ingenieros centrados en el desarrollo y mejora de prótesis visuales implantadas en la corteza visual de pacientes ciegos o con baja visión. El propósito del grupo es lograr que los pacientes humanos alcancen una funcionalidad visual que les permita realizar las tareas habituales de la vida diaria, como la capacidad de reconocer objetos, símbolos numéricos y alfabéticos, así como la capacidad de moverse de forma independiente por el espacio. Para lograr este objetivo, el equipo está involucrado en la optimización del protocolo de implante cortical para cirugía, el desarrollo y diseño de nuevos electrodos que mejoran su biocompatibilidad con el tejido nervioso, así como en el estudio y análisis de las respuestas neurales y perceptivas. de pacientes humanos implantados a la estimulación a través de la neuroprótesis. Estos estudios se complementan con el desarrollo de modelos de retina artificial que intentan reproducir la actividad real de las células ganglionares de la retina en respuesta a la presentación de diferentes estímulos visuales. Adicionalmente, el grupo ha construido una sala de estudio inteligente que permite evaluar la respuesta conductual de los pacientes ante la presentación de estímulos visuales presentados a través de la estimulación de la neuroprótesis visual. La sala de estudio es una reproducción a escala real de un espacio exterior personalizable que permite a los pacientes humanos moverse y navegar por él como si estuvieran paseando por la ciudad y guiados por la presentación de estímulos a través de la neuroprótesis implantada.
Línea 9: Abordaje optogenético en la restauración visual
El surgimiento de la optogenética ha revolucionado el campo de la neurociencia y ha demostrado ser una herramienta invaluable para manipular la actividad en las neuronas a través de la fotoestimulación con alta precisión temporal y especificidad genética dirigida. Los canales fotosensibles como la canalrodpsina-2 (ChR2) y la plétora de variantes de bioingeniería que han surgido no solo funcionan como una herramienta de exploración en neurociencia, sino que también tienen profundas implicaciones en la terapia. Nuestro objetivo es utilizar la optogenética como una alternativa viable y mejorada a los enfoques actuales en la restauración visual en pacientes con retinitis pigmentaria (RP) que han perdido su capa de fotorreceptores. La introducción de proteínas optogenéticas en las capas residuales de la retina puede resultar clínicamente viable como una terapia capaz de cambios significativos y significativos en la calidad de su visión y vida. Expresamos nuevos vatiants optogenéticos mejorados (CatCh y Chrimson) en la retina intacta restante, convirtiendo esencialmente estas células en un nuevo tejido fotorreceptor básico capaz de reiniciar la señal visual y transmitirla a los centros visuales superiores para su procesamiento.
N. Al Qtaish, I. Gallego, A.J. Paredes, I. Villate-Beitia, C. Soto-Sánchez, G. Martínez-Navarrete, M. Sainz-Ramos, T. B. López-Méndez, E. Fernández, G. Puras, J.L. Pedraz.
Nanodiamond Integration into Niosomes as an Emerging and Efficient Gene Therapy Nanoplatform for Central Nervous System Diseases.
ACS Appl. Mater. Interfaces 14(11):13665-13677 (2022).
E. Fernández, A. Alfaro, C. Soto-Sánchez, P. González-López, A.M. Lozano, S. Peña, M.D. Grima, A. Rodil, B. Gómez, X. Chen, P.R. Roelfsema, J.D. Rolston, T.S. Davis, R.A. Normann.
Visual percepts evoked with an intracortical 96-channel microelectrode array inserted in human occipital cortex.
J. Clin. Invest.131(23):e151331 (2021).
X. Chen, F. Wang, E. Fernández, P.R. Roelfsema.
Shape perception via a high-channel-count neuroprosthesis in monkey visual cortex.
Science 370(6521):1191-1196 (2020).
J. Sorinas, M.D. Grima, J.M. Ferrández, E. Fernández.
Identifying Suitable Brain Regions and Trial Size Segmentation for Positive/Negative Emotion Recognition.
Int. J. Neural Syst. 29(2):1850044 (2019).
I. Gallego, I. Villate-Beitia, G. Martínez-Navarrete, M. Menéndez, T. López-Méndez, C. Soto-Sánchez, J. Zárate, G. Puras, E. Fernández, J.L. Pedraz.
Non-viral vectors based on cationic niosomes and minicircle DNA technology enhance gene delivery efficiency for biomedical applications in retinal disorders.
Nanomedicine 17:308-318 (2019).
M. Mashal, N. Attia, G. Martínez-Navarrete, C. Soto-Sánchez, E. Fernández, Grijalvo S, R. Eritja, G. Puras, J.L. Pedraz.
Gene delivery to the rat retina by non-viral vectors based on chloroquine-containing cationic niosomes.
J. Control Release 304:181-190 (2019).
A. Lozano, C. Soto-Sánchez, J. Garrigós, J.J Martínez, J.M: Ferrández, E. Fernández.
A 3D Convolutional Neural Network to Model Retinal Ganglion Cell’s Responses to Light Patterns in Mice.
Int. J. Neural Syst. 28(10):1850043 (2018).
M. Mashal, N. Attia, G. Puras, G. Martínez-Navarrete, E. Fernández, J.L. Pedraz.
Retinal gene delivery enhancement by lycopene incorporation into cationic niosomes based on DOTMA and polysorbate 60.
J. Control Release 254:55-64 (2017).
M. Izquierdo-Serra, A. Bautista-Barrufet, A. Trapero, A. Garrido-Charles, A. Díaz-Tahoces, N. Camarero, S. Pittolo, S. Valbuena, A. Pérez-Jiménez, M. Gay, A. García-Moll, C. Rodríguez-Escrich, J. Lerma, P. de la Villa, E. Fernández, M.Á. Pericàs, A. Llebaria, P. Gorostiza.
Optical control of endogenous receptors and cellular excitability using targeted covalent photoswitches.
Nat. Commun. 7:12221 (2016).
J.M. Ayuso, M. Virumbrales-Muñoz, A. Lacueva, P.M. Lanuza, E. Checa-Chavarria, P. Botella, E. Fernández, M. Doblare, J.S. Allison, R.M. Phillips, J. Pardo, L.J. Fernández, I. Ochoa.
Development and characterization of a microfluidic model of the tumour microenvironment.
Sci. Rep. 6:36086 (2016).
Prótesis visuales activas neurales para restaurar la función visual (H2020). Agencia de financiación: Comisión Europea. Vigencia 2022 – 2024
PI: Eduardo Fernández Jover
Fármacos regulados por la luz para restaurar la vista (HR18-00501). Agencia de financiación: Fundación La Caixa, España. Vigencia 2020 – 2022
PI: Eduardo Fernández Jover
Red europea para la formación integrada de terapias innovadoras para la restauración de la visión. (H2020). Agencia de financiación: Comisión Europea. Vigencia 2020 – 2024
PI: Eduardo Fernández Jover
Marco de modelado computacional para la evaluación de seguridad y eficacia de la estimulación PNS. Agencia de financiación: NSF (USA) y Ministerio de Sanidad. Vigencia 2018 – 2022
PI: Eduardo Fernández Jover
Neurotecnología innovadora para la sociedad.. Agencia de financiación: Netherlands Organisation for Scientific Research. Vigencia 2020 – 2027
PI: Eduardo Fernández Jover
| Responsable | Eduardo Fernández Jover |
RESUMEN DE LA INVESTIGACIÓN
Somos un grupo multidisciplinar compuesto por especialistas en diversos campos como la ingeniería, biología, la informática, la robótica, la medicina, etc. Nuestro principal objetivo es la investigación básica y aplicada en patologías visuales, optogenética, estudio de terapias frente a neuropatías de tipo visual, el diseño y desarrollo de dispositivos y sistemas robóticos que ayuden a mejorar la capacidad cognitiva y comunicativa, la salud y la capacidad física de las personas que padecen discapacidades motrices y sensoriales…
LÍNEAS DE INVESTIGACIÓN
Línea 1: Desarrollo y validación de un modelo de neovascularización coroidal inducido por láser
El modelo de neovascularización coroidea inducida por láser es un método establecido utilizado para evaluar las terapias para la degeneración macular húmeda relacionada con la edad (AMD húmeda), una de las principales causas de ceguera en nuestra población de adultos mayores. El principal objetivo de esta línea es obtener un modelo validado para experimentar terapias y tratamientos para el control y curación de esta patología con la finalidad de pasar en el futuro a fases clínicas en humanos con los tratamientos ensayados en el modelo animal.

Generación de neovascularización mediante un sistema láser en retina de rata tras 7 días.
Línea 2:Terapia oftalmológica mediante RNA de interferencia (siRNA) y anticuerpos monoclonales humanizados para patologías degenerativas retinianas.
Esta línea de investigación se basa en la aplicación de nuevas moléculas basadas en RNA de interferencia y anticuerpos monoclonales humanizados para patologías crónicas como la degeneración macular asociada a la edad (DMAE), la retinopatía diabética y la retinitis pigmentaria, que actualmente carecen de tratamientos satisfactorios.
Línea 3: DRUG4SIGHT: Light-regulated drugs to restore sight
En las enfermedades degenerativas de la retina como la retinitis pigmentosa, las células fotorreceptoras se pierden progresivamente, lo que conduce a una discapacidad visual con opciones de tratamiento limitadas. Esta línea pretende caracterizar una serie de compuestos activos sensibles a la luz que puedan fotosensibilizar la retina, estimulando proteínas aún presentes en la retina degenerada y hacer actuar los receptores remanentes de células no degeneradas.
Línea 4: Nueva generación de lentes intraoculares multifuncionales que permiten la liberación prolongada y controlada de agentes terapéuticos a nivel intraocular (OCULUS)
Para evitar o disminuir efectos asociados a la cirugía de cataratas (dolor, infección, inflamación y posibles hemorragias intraoculares) es necesario administrar diariamente fármacos antiinflamatorios y antiinfecciosos durante al menos 6-8 semanas tras la cirugía. La administración tópica de estos fármacos logra retener menos del 5 % del fármaco aplicado tras atravesar la córnea. Por ello, esta línea de investigación se centra en el desarrollo de nuevas lentes intraoculares que liberan sostenidamente fármacos con el fin de obtener una dosis terapéutica continuada.
Línea 5: Aplicación de biofilms con Timolol para el control de la presión intraocular (OCULIPID)
El glaucoma es una enfermedad visual progresiva cuyo factor de riesgo más importante es la elevación de la presión intraocular. Las formulaciones farmacéuticas oculares actuales presentan inconvenientes en cuanto a su administración y eficacia terapéutica. Esta línea de investigación se centra en la aplicación tópica de biofilms lipídicos formulados con Timolol de liberación prolongada para el control de la presión intraocular en un modelo experimental preclínico de glaucoma de conejo.
Línea 6: Entorno de modelado computacional para la evaluación de la seguridad y eficacia de la estimulación del sistema nervioso periférico
El objetivo de esta línea es desarrollar y poner a disposición de la comunidad científica un marco de modelado computacional modular, integrado y multiescala que permitirá diseñar neuroestimuladores periféricos seguros y eficaces. La consecución de esta línea se realizará mediante la reconstrucción tridimensional de la microestructura de nervios estimulados, a través de secciones histológicas, por un método de disección anatómica asistida por computadora. Con ello se pretende mejorar la descripción de la distribución de las fibras nerviosas, proporcionar una representación 3D precisa de los nervios ciáticos, y desarrollar una base de datos informatizada de la topografía de las fibras nerviosas.
Línea 7: Terapia génica con vectores no virales para el tratamiento de enfermedades neurodegenerativas
A día de hoy, la cura de las enfermedades neurodegenerativas es un problema médico que está lejos de resolverse. Un enfoque para lograr una solución es la capacidad de reemplazar los genes defectuosos involucrados en el desarrollo de tales enfermedades por nuevos genes completamente funcionales capaces de interrumpir su progresión. La terapia génica consiste en la transferencia de material genético exógeno para la modificación de células con fines terapéuticos o de investigación. En colaboración con el grupo NanoBioCel (Grupo de Micro y Nano Tecnologías, Biomateriales y Células) de la Universidad del País Vasco, nuestro grupo está trabajando en el desarrollo de nuevos vectores no virales para transferir material genético al interior de las células del sistema nervioso en Con el fin de encontrar nuevas terapias para enfermedades neurológicas. Las grandes ventajas de los vectores no virales en comparación con otros enfoques son su muy baja o nula respuesta inmunogénica en los organismos receptores, su seguridad biológica y química para científicos y fabricantes, su capacidad para transportar grandes fragmentos genéticos dentro de las células y también , su facilidad de producción, manejo, almacenamiento y bajo costo de producción.
Línea 8: Desarrollo de Neuroprótesis Visuales
El equipo multidisciplinar del NBIO, dirigido por el Prof. Eduardo Fernandez Jover, está formado por un grupo de médicos, cirujanos, biólogos e ingenieros centrados en el desarrollo y mejora de prótesis visuales implantadas en la corteza visual de pacientes ciegos o con baja visión. El propósito del grupo es lograr que los pacientes humanos alcancen una funcionalidad visual que les permita realizar las tareas habituales de la vida diaria, como la capacidad de reconocer objetos, símbolos numéricos y alfabéticos, así como la capacidad de moverse de forma independiente por el espacio. Para lograr este objetivo, el equipo está involucrado en la optimización del protocolo de implante cortical para cirugía, el desarrollo y diseño de nuevos electrodos que mejoran su biocompatibilidad con el tejido nervioso, así como en el estudio y análisis de las respuestas neurales y perceptivas. de pacientes humanos implantados a la estimulación a través de la neuroprótesis. Estos estudios se complementan con el desarrollo de modelos de retina artificial que intentan reproducir la actividad real de las células ganglionares de la retina en respuesta a la presentación de diferentes estímulos visuales. Adicionalmente, el grupo ha construido una sala de estudio inteligente que permite evaluar la respuesta conductual de los pacientes ante la presentación de estímulos visuales presentados a través de la estimulación de la neuroprótesis visual. La sala de estudio es una reproducción a escala real de un espacio exterior personalizable que permite a los pacientes humanos moverse y navegar por él como si estuvieran paseando por la ciudad y guiados por la presentación de estímulos a través de la neuroprótesis implantada.
Línea 9: Abordaje optogenético en la restauración visual
El surgimiento de la optogenética ha revolucionado el campo de la neurociencia y ha demostrado ser una herramienta invaluable para manipular la actividad en las neuronas a través de la fotoestimulación con alta precisión temporal y especificidad genética dirigida. Los canales fotosensibles como la canalrodpsina-2 (ChR2) y la plétora de variantes de bioingeniería que han surgido no solo funcionan como una herramienta de exploración en neurociencia, sino que también tienen profundas implicaciones en la terapia. Nuestro objetivo es utilizar la optogenética como una alternativa viable y mejorada a los enfoques actuales en la restauración visual en pacientes con retinitis pigmentaria (RP) que han perdido su capa de fotorreceptores. La introducción de proteínas optogenéticas en las capas residuales de la retina puede resultar clínicamente viable como una terapia capaz de cambios significativos y significativos en la calidad de su visión y vida. Expresamos nuevos vatiants optogenéticos mejorados (CatCh y Chrimson) en la retina intacta restante, convirtiendo esencialmente estas células en un nuevo tejido fotorreceptor básico capaz de reiniciar la señal visual y transmitirla a los centros visuales superiores para su procesamiento.
N. Al Qtaish, I. Gallego, A.J. Paredes, I. Villate-Beitia, C. Soto-Sánchez, G. Martínez-Navarrete, M. Sainz-Ramos, T. B. López-Méndez, E. Fernández, G. Puras, J.L. Pedraz.
Nanodiamond Integration into Niosomes as an Emerging and Efficient Gene Therapy Nanoplatform for Central Nervous System Diseases.
ACS Appl. Mater. Interfaces 14(11):13665-13677 (2022).
E. Fernández, A. Alfaro, C. Soto-Sánchez, P. González-López, A.M. Lozano, S. Peña, M.D. Grima, A. Rodil, B. Gómez, X. Chen, P.R. Roelfsema, J.D. Rolston, T.S. Davis, R.A. Normann.
Visual percepts evoked with an intracortical 96-channel microelectrode array inserted in human occipital cortex.
J. Clin. Invest.131(23):e151331 (2021).
X. Chen, F. Wang, E. Fernández, P.R. Roelfsema.
Shape perception via a high-channel-count neuroprosthesis in monkey visual cortex.
Science 370(6521):1191-1196 (2020).
J. Sorinas, M.D. Grima, J.M. Ferrández, E. Fernández.
Identifying Suitable Brain Regions and Trial Size Segmentation for Positive/Negative Emotion Recognition.
Int. J. Neural Syst. 29(2):1850044 (2019).
I. Gallego, I. Villate-Beitia, G. Martínez-Navarrete, M. Menéndez, T. López-Méndez, C. Soto-Sánchez, J. Zárate, G. Puras, E. Fernández, J.L. Pedraz.
Non-viral vectors based on cationic niosomes and minicircle DNA technology enhance gene delivery efficiency for biomedical applications in retinal disorders.
Nanomedicine 17:308-318 (2019).
M. Mashal, N. Attia, G. Martínez-Navarrete, C. Soto-Sánchez, E. Fernández, Grijalvo S, R. Eritja, G. Puras, J.L. Pedraz.
Gene delivery to the rat retina by non-viral vectors based on chloroquine-containing cationic niosomes.
J. Control Release 304:181-190 (2019).
A. Lozano, C. Soto-Sánchez, J. Garrigós, J.J Martínez, J.M: Ferrández, E. Fernández.
A 3D Convolutional Neural Network to Model Retinal Ganglion Cell’s Responses to Light Patterns in Mice.
Int. J. Neural Syst. 28(10):1850043 (2018).
M. Mashal, N. Attia, G. Puras, G. Martínez-Navarrete, E. Fernández, J.L. Pedraz.
Retinal gene delivery enhancement by lycopene incorporation into cationic niosomes based on DOTMA and polysorbate 60.
J. Control Release 254:55-64 (2017).
M. Izquierdo-Serra, A. Bautista-Barrufet, A. Trapero, A. Garrido-Charles, A. Díaz-Tahoces, N. Camarero, S. Pittolo, S. Valbuena, A. Pérez-Jiménez, M. Gay, A. García-Moll, C. Rodríguez-Escrich, J. Lerma, P. de la Villa, E. Fernández, M.Á. Pericàs, A. Llebaria, P. Gorostiza.
Optical control of endogenous receptors and cellular excitability using targeted covalent photoswitches.
Nat. Commun. 7:12221 (2016).
J.M. Ayuso, M. Virumbrales-Muñoz, A. Lacueva, P.M. Lanuza, E. Checa-Chavarria, P. Botella, E. Fernández, M. Doblare, J.S. Allison, R.M. Phillips, J. Pardo, L.J. Fernández, I. Ochoa.
Development and characterization of a microfluidic model of the tumour microenvironment.
Sci. Rep. 6:36086 (2016).
Prótesis visuales activas neurales para restaurar la función visual (H2020). Agencia de financiación: Comisión Europea. Vigencia 2022 – 2024
PI: Eduardo Fernández Jover
Fármacos regulados por la luz para restaurar la vista (HR18-00501). Agencia de financiación: Fundación La Caixa, España. Vigencia 2020 – 2022
PI: Eduardo Fernández Jover
Red europea para la formación integrada de terapias innovadoras para la restauración de la visión. (H2020). Agencia de financiación: Comisión Europea. Vigencia 2020 – 2024
PI: Eduardo Fernández Jover
Marco de modelado computacional para la evaluación de seguridad y eficacia de la estimulación PNS. Agencia de financiación: NSF (USA) y Ministerio de Sanidad. Vigencia 2018 – 2022
PI: Eduardo Fernández Jover
Neurotecnología innovadora para la sociedad.. Agencia de financiación: Netherlands Organisation for Scientific Research. Vigencia 2020 – 2027
PI: Eduardo Fernández Jover
Desarrollo de una nueva generación de prótesis corticales con el sistema visual. Agencia de financiación: Ministerio de Ciencia, España. Vigencia 2019 – 2022
PI: Eduardo Fernández Jover
Validación clínica de una neuroprótesis visual cortical para ciegos basada en microelectrodos intracorticales.. Agencia de financiación: Generalitat Valenciana, España. Vigencia 2019 – 2022
PI: Eduardo Fernández Jover
